在化学气相沉积(CVD)中,前驱体分子的生成和随后的分解受热力学和动力学的基本原理支配。您能够通过调节温度、压力和浓度等工艺参数来控制这两种力量之间的相互作用,这直接决定了最终薄膜的质量、结构和生长速率。
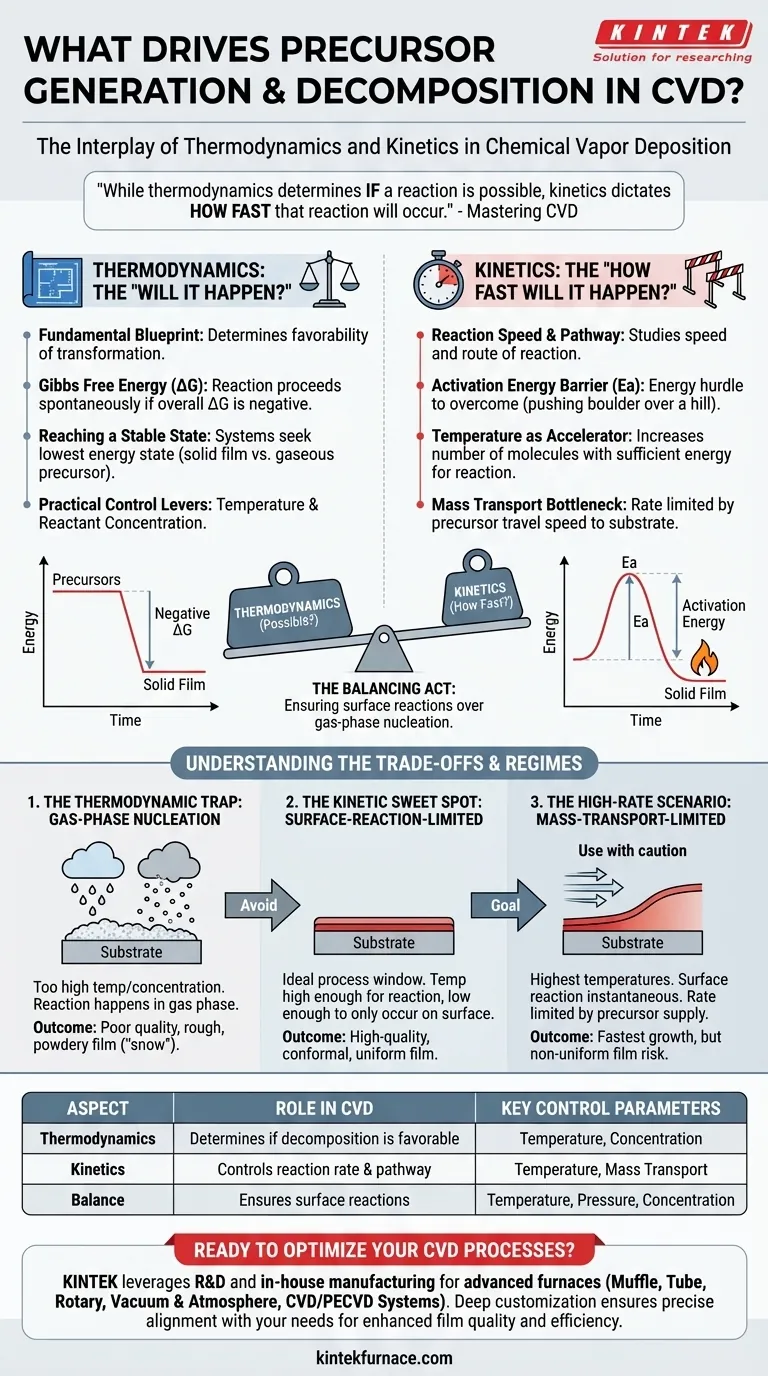
热力学决定了反应是否可能发生及其最稳定的结果,而动力学则决定了反应发生多快。掌握CVD是一个寻找动力学最佳点(即反应在衬底表面可控地发生,而不是在气相中混乱发生)的过程。
热力学的作用:“它会发生吗?”
热力学为任何化学反应提供了基本蓝图,包括CVD过程中的反应。它告诉您在您的设定条件下,从气态前驱体到固态薄膜的所需转变是否有利。
吉布斯自由能 (ΔG)
热力学有利性的主要指标是吉布斯自由能变化 (ΔG)。只有当总 ΔG 为负时,反应才能自发进行。
在CVD中,这意味着系统必须倾向于前驱体分解成稳定的固态薄膜和气态副产物的状态,而不是它们保持为完整前驱体分子的状态。
达到稳定状态
所有系统都自然寻求其最低能量状态。通过向CVD反应器引入能量(通常是热量),您使前驱体分子能够克服障碍,并在衬底上重新排列成更稳定的固态薄膜结构。
实际控制杆
您主要通过温度和反应物浓度来影响系统的热力学。升高温度通常会使分解反应更有利(ΔG 更负),推动平衡向产物形成方向移动。

动力学的作用:“它会发生多快?”
一个反应在热力学上可行并不意味着它会以有用的速率发生。动力学是研究反应速度和反应路径的学科。
活化能垒 (Ea)
前驱体要分解,必须克服一个被称为活化能(Ea)的能量障碍。可以想象成需要将一块巨石推过一座小山才能滚入一个深谷。
即使山谷(固态薄膜)是能量更低的状态,如果没有足够的能量越过最初的山丘,反应也不会发生。
温度作为加速器
温度是控制动力学最有力的工具。升高温度会使更多分子获得克服活化能垒所需的能量,从而显著提高反应速率。
传质瓶颈
动力学不仅仅关乎化学反应本身。整体速率也可能受到传质的限制——前驱体分子通过气相到达衬底表面的速度。
理解权衡
CVD过程的成功取决于平衡热力学和动力学,以使表面反应优于气相反应。这种平衡定义了您的过程的操作范围。
热力学陷阱:气相成核
如果温度或浓度过高,反应会变得过快,并且在任何地方都热力学有利。前驱体在到达衬底之前就会在热气相中反应。
这种气相成核会形成微小的固体颗粒(“雪”或粉末),它们可能会落在您的衬底上,导致薄膜粗糙、附着力差且质量低劣。
动力学最佳点:表面反应限制区域
理想的工艺窗口通常是表面反应限制区域。在此区域,温度足够高以使反应发生,但又足够低以确保它们只在具有催化活性的衬底表面发生。
在这种动力学控制的状态下,薄膜生长是均匀有序的,因为表面化学反应速率是过程中最慢的步骤。
高速情景:传质限制区域
在更高的温度下,表面反应变得瞬时。生长速率现在仅受限于新前驱体分子到达表面的速度。
这种传质限制区域提供了最快的生长速度,但存在产生不均匀薄膜的固有风险,因为气体流动较好的区域(例如晶圆的前缘)将生长出更厚的层。
为您的目标做出正确选择
您的工艺参数应根据薄膜的预期结果进行设置。
- 如果您的主要关注点是高质量、共形且均匀的薄膜:通过仔细控制温度,在表面反应限制区域操作,以确保反应发生在衬底上,而不是在气体中。
- 如果您的主要关注点是最大沉积速率:您需要将温度推入传质限制区域,但必须接受固有的不均匀性风险。
- 如果您观察到颗粒形成或薄膜模糊:您的工艺可能过于激进。降低温度或前驱体浓度,以脱离气相成核区域。
最终,掌握“可能发生什么”(热力学)与“以受控速率发生什么”(动力学)之间的平衡是成功进行化学气相沉积的关键。
总结表:
| 方面 | 在CVD中的作用 | 关键控制参数 |
|---|---|---|
| 热力学 | 决定前驱体分解是否有利 | 温度、浓度 |
| 动力学 | 控制反应速率和路径 | 温度、传质 |
| 平衡 | 确保表面反应优于气相成核 | 温度、压力、浓度 |
准备好使用定制的高温炉解决方案优化您的CVD工艺了吗? KINTEK凭借卓越的研发和内部制造能力,提供先进的炉型,如马弗炉、管式炉、旋转炉、真空和气氛炉以及CVD/PECVD系统。我们深入的定制能力确保与您独特的实验需求精确对齐,从而提高薄膜质量和效率。立即联系我们,讨论我们如何支持您的实验室目标!
图解指南
相关产品
- 定制多功能 CVD 管式炉 化学气相沉积 CVD 设备机
- 带真空站 CVD 设备的分室式 CVD 管式炉
- 用于化学气相沉积设备的多加热区 CVD 管式炉设备
- 滑轨式 PECVD 管式炉(带液体汽化器 PECVD 机)
- 倾斜旋转等离子体增强化学气相沉积 PECVD 管式炉



















